Phát hiện thấy 24 nội dung liên quan đến chủ đề hóa 8 bài 2.


.PNG)






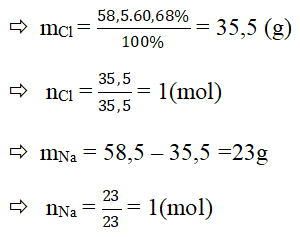






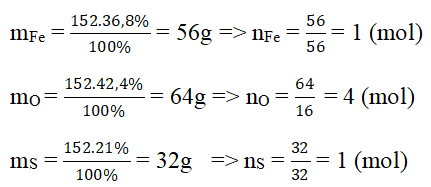



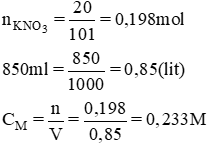


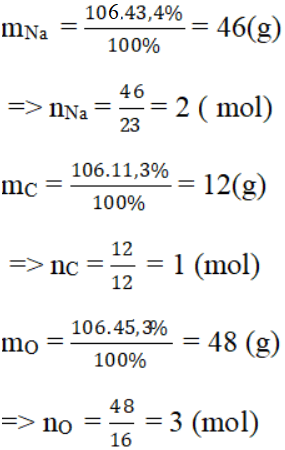

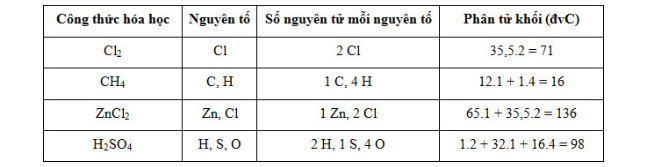
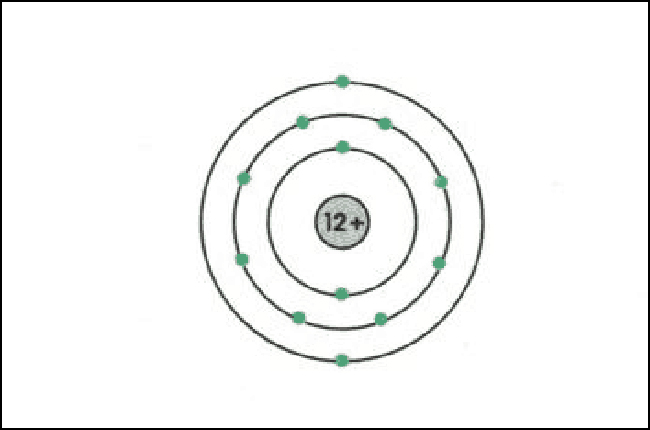
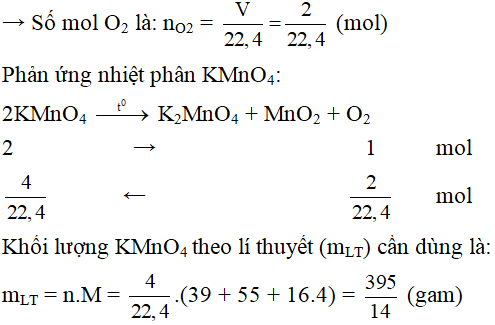













.png)


hóa 8 bài 2
Các khái niệm chính của bài học Hóa 8 Bài 2
Phản ứng lưỡng tính và phản ứng một chiều: Phản ứng lưỡng tính là phản ứng mà các chất trong phản ứng có khả năng tác dụng với nhau và tạo ra sản phẩm. Trong phản ứng lưỡng tính, cung cấp chất tác dụng với một lượng nhỏ sẽ gây ra sự thay đổi tức thì và không có sự thay đổi dài hạn trong hệ thống phản ứng. Phản ứng một chiều là phản ứng mà các chất chỉ tác dụng với nhau một chiều và không có sự cân bằng giữa chất đầu vào và sản phẩm.
Cân bằng hóa học và định luật bảo toàn khối lượng: Cân bằng hóa học là một trạng thái ổn định trong hệ thống phản ứng, trong đó số lượng chất đầu vào và sản phẩm là không đổi. Định luật bảo toàn khối lượng là một nguyên tắc cho biết khối lượng chất đầu vào và sản phẩm phản ứng bằng nhau.
Hằng số cân bằng và ảnh hưởng của nhiệt độ đến cân bằng hóa học: Hằng số cân bằng là một giá trị hằng số mô tả một phản ứng hóa học lưu giữ trong trạng thái cân bằng. Nhiệt độ ảnh hưởng đến hằng số cân bằng và sự cân bằng của phản ứng hóa học.
Cách giải quyết bài tập Hóa 8 Bài 2
Để giải quyết bài tập Hóa 8 Bài 2, trước tiên bạn cần hiểu rõ yêu cầu đề bài và các khái niệm liên quan. Sau đó, bạn cần sử dụng công thức cân bằng để tính toán nồng độ các chất trong phản ứng. Kế đó, dựa vào hằng số cân bằng để giải quyết các câu hỏi trong bài tập.
Các lưu ý khi làm bài tập Hóa 8 Bài 2
Khi làm bài tập Hóa 8 Bài 2, bạn cần chú ý đến tình trạng phản ứng và xác định loại phản ứng. Ngoài ra, bạn cần sử dụng định luật bảo toàn khối lượng và công thức cân bằng để giải quyết phản ứng. Đọc đề bài kỹ càng để tránh mắc sai lầm khi giải toán.
Các ví dụ về bài tập Hóa 8 Bài 2
Một ví dụ về bài tập tính toán nồng độ chất trong phản ứng lưỡng tính là: Cho 10g Fe3O4 tác dụng với HCl. Tính khối lượng Cl2 được sinh ra và khối lượng muối FeCl2 tạo thành.
Một ví dụ về bài tập ứng dụng định luật bảo toàn khối lượng và công thức cân bằng để giải quyết phản ứng trong thực tế là: Cho biết phản ứng cháy hoàn toàn hỗn hợp X hoàn toàn thành CO2 và H2O. Biết khối lượng mỗi 1 mol CO2 và 1 mol H2O lần lượt là 44g và 18g. Tính khối lượng X và khối lượng O2 cần thiết để cháy hết X.
Một ví dụ về bài tập tính toán ảnh hưởng của nhiệt độ đến hằng số cân bằng và cân bằng hóa học là: Cho biết phản ứng giữa SO2 và O2 tạo thành SO3 có công thức cân bằng: 2SO2 + O2 ⇌ 2SO3. Biết ΔHr = -197kJ/mol. Tính giá trị hằng số cân bằng Kp và Kc của phản ứng ở nhiệt độ 25oC, nếu áp suất bên trong bình là 5 atm.
Từ khoá người dùng tìm kiếm: hóa 8 bài 2 Hóa 8 Bài 3, Hóa 8 bài 2 trang 57, Hóa 8 Bài 21, Hóa học 8 Bài 1, Hóa 8 bài 2 trang 71, Hóa 8 Bài 20, Hóa 8 Bài 4, Hóa học 8 Bài 2 lý thuyết
Chất – Bài 2 – Hóa học 8 – Cô Nguyễn Thị Thu (HAY NHẤT)
Xem thêm tại đây: nhanvietluanvan.com
Link bài viết: hóa 8 bài 2.
Xem thêm thông tin về chủ đề hóa 8 bài 2.
- Giải Hóa 8 bài 2: Chất – VietJack.com
- Bài 2. Chất – Loigiaihay.com
- Hoá học 8 Bài 2: Chất Giải Hoá học lớp 8 trang 11
- Giải bài 2 hóa học 8: Chất – Tech12h
- Hướng dẫn giải bài tập hóa học 8 bài 2 siêu chi tiết dễ hiểu nhất
- Giải hóa 8 bài 2: Chất | Giải môn Hóa học lớp 8 – soanvan.net
Categories: nhanvietluanvan.com/imgi
